本文作者:陆可馨
「希望上班第一天不要太忙啊。」
端午假期后的第一天,我早早坐在办公室,一边在心里默默祈祷着,一边打开电脑缓慢启动自己的工作状态。
「陆姐!你来啦!」师妹突然出现在我的背后。
「太阳打西边出来了,你怎么来的比我还早?」我调侃道。
「别提了陆姐。」师妹露出一张苦瓜脸,「昨晚被喊回来加班加到现在的,还记得咱们心内科『常客』丁大爷不?」
「怎么回事?」我顿时觉得有些不妙。
丁大爷是市里某个科研院所的退休工程师,自打退休以来就在我们医院的门诊看病了。丁大爷平日里谈吐颇有学者风范,而且坚持十几年风雨无阻地来医院复查,一来二去,他也成为了我们口中的「模范病人」。
不仅如此,他还是我迄今为止见过病程最长的肥厚型心肌病患者——从 20 多岁确诊,到如今 78 岁高龄,已经超过 50 年。
「丁大爷昨晚心衰被 120 送急诊去了,急诊推了速尿没效果,后半夜转进来住院了。」
「现在情况呢?」
「泵了米力农和新活素,没啥大事了。」
虽然存在心力衰竭的情况,但丁大爷的生活质量一直还可以,近年来的病情也比较稳定。为什么会突发心衰?问题到底有多严重?我暗自担心着,点开了丁大爷本次入院的病程记录。
01.
78 岁高龄,丁大爷的健康状况一直也不简单。
除了年轻时就确诊的心肌病和高血压,丁大爷的诊断中还包含冠心病、心律失常、肾功能不全、白内障和前列腺肥大等疾病。好在丁大爷和家属的依从性极高,这些疾病都得到了及时的诊疗和有效的控制。
不过,当我点开超声心动图报告时,却有了一点出乎预料的发现。
「陆姐,我就是想问这个,一般的肥厚型心肌病是单纯左心室肥厚对吧,为什么这个的右室我看着也像增厚了呢?还有二尖瓣,也像有点增厚。」师妹率先发出疑问。
「也有的会同时在心尖处存在心肌肥厚[1],或者是心腔中部出现心肌病变[2]。」我回答道,「但你说的没错,像这样同时双心室室壁肥厚,还出现二尖瓣增厚的情况是极其罕见的。」
「看看他之前的心超就知道了。」师妹说着打开了另一台电脑的门诊病历系统。我凑过去一看,她已经找到了丁大爷 10 年前在我院留下的第一份病例——这几乎是我院最早电子化的第一批病历了。
2013 年,丁大爷来到我科就诊,抱怨走路后经常出现胸部不适和呼吸困难,小腿也开始浮肿起来。
接诊医生考虑到丁大爷的肥厚型心肌病病史,认为可能是疾病加重引起的症状,在丁大爷每天服用美托洛尔和氨氯地平的基础上,又增开了依那普利每日服用,并嘱咐丁大爷在水肿严重时吃一片复方阿米洛利。
第二份病例的时间是 2014 年。这次,丁大爷因为恶心、头晕和胸部不适就诊,心电图发现了三度房室传导阻滞和明显的心动过缓,随后入院接受手术,植入了一枚双腔植入型心律转复除颤器。
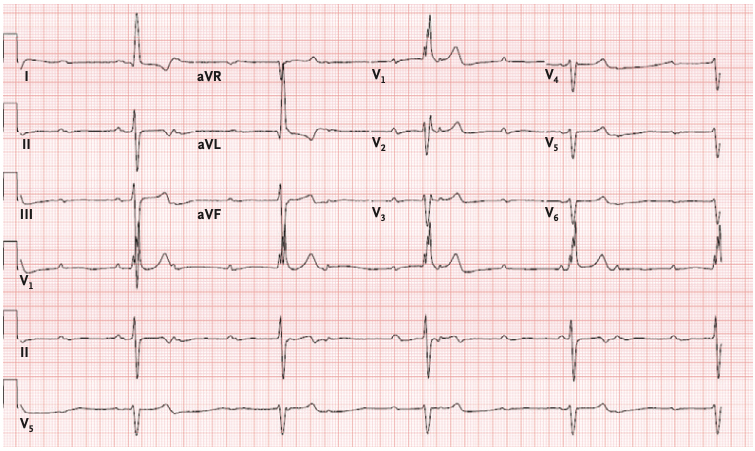
患者心电图显示房室传导阻滞和心动过缓(图源:参考资料 11)
「植入除颤器?这个时候丁大爷还没有出现心动过速吧?」师妹再次感到不解。
「现在的除颤器大多数是带有起搏功能的,对于丁大爷这种有致命性心律失常风险的心肌病患者来说,植入除颤器可比植入起搏器划算太多了。」我说。
继续看下去。手术后 4 个月,丁大爷出现了房颤,虽然第一次房颤复律成功,但 3 天后房颤复发,这次医生开出了胺碘酮和华法林长期治疗。
此后很长的一段时间,丁大爷虽然隔三差五来复诊,但病历基本上都是流水账,他的心脏情况一直稳定得很,直到距今 2019 年的一次复诊,丁大爷因「肺水肿」再次进了医院。
「这个我记得!」师妹说,「当时我在跟老板门诊,好像家属说是出去旅游吃得太咸了还是怎么的,总之利尿剂治疗后就好转了,基本没什么大的影响。」
不过,也正是这次就诊后,丁大爷的心脏情况就逐渐开始走下坡路:一爬楼梯或者走斜坡就会出现呼吸困难、极度疲惫,晚上睡觉还经常需要枕两个枕头才能安稳入睡,更糟糕的是,复查时主任程控除颤器发现丁大爷存在间歇性的室性心动过速。
联系到本次心超中不同寻常的表现,我和师妹都有了不妙的预感。
02.
医生办公室门外突然传来一阵嘈杂,我回头看去。
「实习生吗?完了!今天入科来着,我还没准备好 SP。」师妹赶紧跳起来。(SP,standard patient:标准化病人,用于医学教育、医疗专业人员的评估。)
我沉思片刻:「正好,丁大爷和他家人和我们科室都比较熟,配合度也高,你去问问,方便的话带同学们练习病史询问吧。」
一个多小时后,师妹带着一群小孩儿浩浩荡荡地回到办公室。
我和师妹快速交换眼神:咋样?还不错。
实习生就座后,一位男生主动站起来:「我们组派我做代表,整理了一下患者的病史。」我点头示意他继续讲下去。
男生清了清嗓:「首先,丁爷爷的人生堪称传奇。」
我再次和师妹快速交换眼神:你教的?我不是,我没有。
男生继续讲下去,时间回到 58 年前。
20 岁以前,丁大爷——或者应该说「小丁」——还没有受到心脏疾病的困扰。那时,小丁不仅学习成绩优秀,运动水平也一流,不仅是校田径队的成员,还在校运会上打破过百米短跑记录。
然而,在 21 岁的某一天,小丁在校队训练突发小腿麻木刺痛。起初,他并没有太当回事,但休整了一段时间后,症状不仅没有减轻,他还发现自己脚上和腿上的出汗量明显减少。然而,皮肤科的医生也并没有给出明确诊断,小丁的运动成绩受到伤病影响一路下滑。
一次短跑训练后,小丁突然感到头晕难忍,被同学们送往医院。也正是在这一次,他被心内科医生首次诊断出肥厚型心肌病。好在当时,小丁的病情并不严重,除了不能再踏入自己热爱的跑道,他还是顺利的结婚生子。
随着岁月增长,小丁逐渐变成「老丁」,疾病对身体的影响也越来越明显。53 岁那年,老丁在单位体检中被查出左心室肥大和高血压,心超显示左心室壁对称性增厚至 19mm(正常值≤11mm),并同时存在二尖瓣增厚和二尖瓣反流。随后,老丁开始常规服用治疗心肌病的美托洛尔和治疗高血压的氨氯地平。
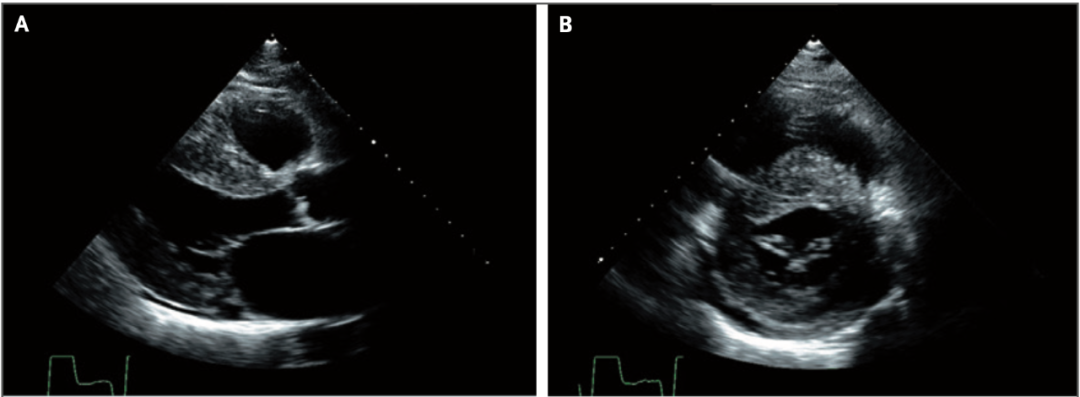
心超示心肌肥厚(图源:参考资料 11)
此后多年,老丁的情况倒也一直稳定,直到退休后,已经成为「丁大爷」的他开始在离家最近的我院定期复诊……后面的故事,就是我们在门诊系统里看到的内容了。
03.
听完实习生的病史汇报,我对其中几个疑点陷入了沉思:
首先,是丁大爷 20 岁初曾经出现的腿部少汗、麻木刺痛症状,是下肢周围神经病吗?
其次,丁大爷的左心室肥厚和高血压似乎是同时出现的,而且连续多次的心超检查均未发现肥厚型心肌病中常见的左心室流出道梗阻,这又意味着什么?
此外,在等待病史问询的过程中,我又回顾了丁大爷近几年的门诊和住院检验报告记录,发现他的肌酐和尿素氮水平逐步隐匿升高,截至这次住院,丁大爷已经发展成了伴白蛋白尿的轻度肾功能不全。
心脏传导异常,双心室壁增厚心肌病,周围神经病,肾病......种种不寻常,是不同疾病的巧合吗?不,我很快否定了这个念头。无论患者有多少症状、多少异常体征,还是应该尽可能用一种疾病来穿起整个框架,这是「医学一元论」的基本原则。
那么,对于丁大爷的种种症状,什么才是突破口?
「啊对了老师!刚刚忘记说家族史。」汇报的男生打断了我的思路,「根据患者和家属的描述,丁爷爷的姐姐、妹妹,以及他的外甥女也都患有肥厚型心肌病,而其他家属,包括儿子、两个孙子都没什么大问题。」
我一下子顿住了:长达 58 年的肥厚型心肌病病史、长达 10 年的我科随访病史、我对患者的了解等等因素,让我都陷入了惯性思维,反而忽略了最基本的问题……
04.
安顿好实习生的任务,师妹迅速回到电脑前:「陆姐,你是不是想到什么了?」
我点点头:「肥厚型心肌病是常染色体显性遗传[3],但是丁大爷这个家族史很难不让人在意。」
「传男不传女,X 连锁遗传?」师妹抢答道。
我点点头:「但因为是老病人,在之前的门诊随访中,我们很少关注到这点,患者也没怎么提过……结合他的症状,我目前想到了两个可能。」
首先是淀粉样变性。
凑巧的是,我前段时间刚刚参与了一例与内分泌科会诊的遗传性转甲状腺素蛋白淀粉样变性,其缓慢温和的病程可以解释丁大爷的部分症状,但是,该病患者的胃肠道症状往往非常严重[4],而丁大爷没有这方面的困扰;而更为凶险的免疫球蛋白轻链淀粉样变性,患者生存期非常短[5],恐怕撑不到今天。
其次是溶酶体贮积病(LSD)。
如果考虑到可能的 X 连锁遗传,LSD 有三种符合标准:达农病、法布雷病和黏多糖贮积症 II 型[6]。
达农病患者虽然普遍存在类似于肥厚型心肌病的心脏表现,但该病的男性患者早至 12 岁即可发病,且几乎均存在智力障碍和肌无力[7];黏多糖贮积症 II 型患者则有典型的皮肤病变、中枢神经受累和面容异常[8]……
那么,法布雷病呢?
和其他 LSD 一样,法布雷病也是溶酶体内清除特定化合物的酶活性大幅降低或缺失,引起有毒化合物累积,从而损伤特定细胞和器官。
在法布雷病患者中,溶酶体 α-半乳糖苷酶 A 的活性缺失导致酰基鞘鞍醇三己糖(Gb3)在多种细胞的溶酶体中蓄积,而 Gb3 蓄积后会进一步转化为有毒的亲水性去酰化衍生物,从而产生细胞毒性、促炎性和促纤维化等多种有害效应。
Gb3 常蓄积于自主神经节、后根神经节、肾小球、肾小管和肾间质细胞、心肌细胞、血管平滑肌细胞、角膜内血管内皮细胞和淋巴管内皮细胞、瓣膜纤维细胞和心脏传导纤维。因此,法布雷病主要累及外周神经系统、皮肤与毛细血管、眼部、脑血管、心脏(包括心脏瓣膜、心脏传导系统和心肌)、肾脏等部位。
由于 Gb3 的蓄积、向有毒产物转化和发挥细胞毒性的一系列过程在组织间存在差异,法布雷病的症状通常随年龄增长序贯出现。
「这样看来,很有必要做个基因检测了。」师妹总结道。
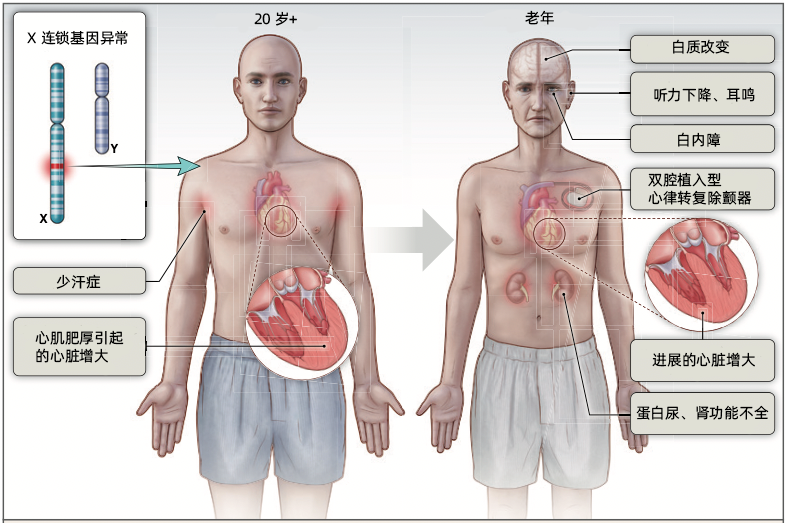
丁大爷症状示意图(图源:参考文献 11 插图编译)
05.
在和丁大爷及家属进行沟通后,我们很快签署了知情同意,并为丁大爷联系了遗传病检测实验室。
15 天后,我收到了实验室传来的两份检测报告。其中的基因检测报告显示,丁大爷的 GLA 基因(该基因编码溶酶体 α-半乳糖苷酶 A)外显子 6 上检测到 R301G 突变,该突变已知可导致法布雷病;另一份酶活性检测报告显示,丁大爷的血浆样本中未检测到 α-半乳糖苷酶 A 的残留活性,证实丁大爷为经典型法布雷病患者。
真相大白,我却并没有为此感到开心。
有近年研究显示,在我国肥厚型心肌病患者中,法布雷病的发生率约为 0.93%,这不是一个小数字。但由于症状多样且缺乏特异性,法布雷病依然经常被误诊和漏诊。
相比治疗手段有限的肥厚型心肌病,法布雷病虽然累及全身多系统,但早就有了治疗方案。
根据 2013 年的《中国法布雷病(Fabry 病)诊治专家共识》,酶替代治疗——即利用基因重组技术体外合成 α-Gal A 替代体内缺陷的酶——可以很大程度上减轻甚至避免心脏和肾脏的病变。
多个随机对照及开放扩展临床试验结果均显示重组人类 α-Gal A 替代治疗法布里病可减少患者细胞内 GL3 的沉积,有效减轻患者的肢端疼痛、胃肠道症状,改善心肌肥厚,稳定肾功能,从而改善患者的生活质量和预后。
但是,对于丁大爷来说,这份真相来得有些太晚了。
《中国法布雷病(Fabry 病)诊治专家共识》中提到,一般来说,法布雷病的患者往往在儿童至青少年时期就出现临床症状,并随病程进展而逐渐加重,许多患者尤其是男性患者常在中青年死于严重的肾功能衰竭或心脑血管并发症。
丁大爷这样一位活到了 78 岁高龄的法布雷病患者,实属罕见。
但同样,对于 78 岁高龄的丁大爷来说,心脏病已经进入了不可逆阶段,虽说短期内不至于危及生命,但积极治疗也无法逆转病变。
更揪心的是,此前丁大爷为了治疗房颤而服用的胺碘酮,可能通过在溶酶体中竞争性抑制磷脂酶 A2[10]而加速法布雷病的进展,丁大爷的心肌病在房颤过后不断加重,也不能完全排除与胺碘酮有关。
这个「救命」的药物,实际上却加重了他的症状。
好在,当开始怀疑法布雷病的时候,我们已经第一时间为丁大爷暂停了胺碘酮的医嘱。经过和丁大爷及家属的沟通,我们为丁大爷调整治疗方案,很快,他的病情稳定得以出院。未来,丁大爷的家属、后代也可以通过遗传咨询而避免法布雷病的影响。
但我依然会想,在这段横跨了 58 年的病程里,在丁大爷随访的 10 年时间里,如果有人能早一点察觉到蛛丝马迹,那么,结果是否会截然不同呢?(策划:z_popeye|监制:carellero)
致谢:本文经 中山大学孙逸仙纪念医院心血管内科副主任医师 麦憬霆 专业审核
未经允许不得转载:澳鸟-全球资讯平台 » 漏诊 58 年,确诊后医生冲向电脑:急停这个医嘱

 澳鸟-全球资讯平台
澳鸟-全球资讯平台









